Muchos protozoos viven en el cuerpo humano. Muchos de ellos son patógenos. Nuestra historia es sobre diez de ellos, la mayoría. La revisión se basa en publicaciones históricas y recientes.
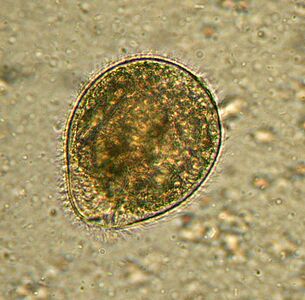
Más grande. BalantidiumBalantidium coli
El protozoario más grande es un parásito humano y el único ciliado de esta compañía. Sus dimensiones varían de 30 a 150 micrones de largo y de 25 a 120 micrones de ancho. A modo de comparación: la longitud del plasmodio de la malaria en la etapa más grande es de aproximadamente 15 micrones, y varias veces menor que el balantidium de las células intestinales, entre las cuales viven los ciliados. Un elefante en una tienda de porcelana.
Distribuidodondequiera que haya cerdos, sus principales portadores. Habitualmente vive en la capa submucosa del colon, aunque en humanos también ocurre en el epitelio pulmonar. Se alimenta de bacteriasB. coli, partículas de alimentos y fragmentos del epitelio del huésped. En los animales, la infección es asintomática. Las personas pueden desarrollar diarrea intensa con secreción viscosa y sanguinolenta (balantidiasis), a veces se forman úlceras en las paredes del colon. Es raro morir de balantidiasis, pero provoca agotamiento crónico.
Las personas se infectan a través del agua sucia o alimentos que contienen quistes. La tasa de infección en humanos no supera el 1%, mientras que los cerdos pueden infectarse en todo el mundo.
Tratadocon antibióticos, todavía no se han reportado informes de resistencia a los medicamentos de este cilio.
Descubiertopor el científico sueco Malstem en 1857. Hoy en día, la balantidiasis está asociada con áreas tropicales y subtropicales, pobreza y mala higiene.
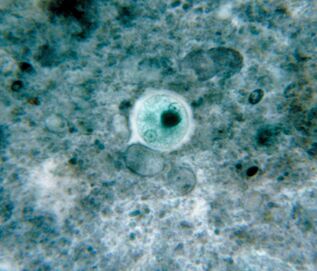
El primero. Ameba oralEntamoeba gingivalis
La primera ameba parasitaria encontrada en humanos. La descripción de las amebas se publicó en 1849 en la revista científica más antigua. Ameba encontrada en la placa dental, de ahí el nombre del latín gingivae - encías.
Viveen la boca de casi todas las personas con dolor de muelas o encías, habita en las bolsas de las encías y en la placa. Se alimenta de células epiteliales, leucocitos, microbios y en el caso de eritrocitos. Es raro en personas con una cavidad bucal sana.
Este pequeño protozoo, de 10 a 35 µm de tamaño, no sale al medio ambiente y no forma quistes, se transmite a otro huésped por besos, a través de platos sucios o alimentos contaminados. E. gingivalisse considera un parásito exclusivamente humano, pero a veces se encuentra en gatos, perros, caballos y monos cautivos.
A principios del siglo XX,E. gingivalisse describió como el agente causante de la enfermedad periodontal, ya que siempre está presente en las células dentales inflamadas. Sin embargo, no se ha demostrado su patogenicidad.
Se desconocen los fármacosque afectan a esta ameba.
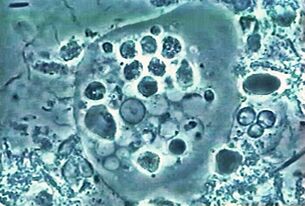
El más omnipresente. Ameba de disenteríaEntamoeba histolytica
Este parásito intestinal con sangre penetra en los tejidos del hígado, pulmones, riñones, cerebro, corazón, bazo, genitales. Come lo que obtiene: partículas de alimentos, bacterias, glóbulos rojos, leucocitos y células epiteliales.
Distribuidoen todas partes, especialmente en los trópicos. Por lo general, las personas se infectan al tragar un quiste.
En los países templados, la ameba suele permanecer en la luz intestinal y la infección es asintomática. En los trópicos y subtrópicos, el proceso patológico a menudo comienza:E. histolyticaataca las paredes. Las razones de la transición a la forma patógena aún no están claras, pero ya se han descrito varios mecanismos moleculares de lo que está sucediendo. Por lo tanto, está claro que las amebas secretan sustancias de lisis, atraviesan el moco y matan las células. Aparentemente, la ameba puede destruir la célula huésped de dos maneras: desencadenando la apoptosis en ella o simplemente masticando pedazos. El primer método se consideró el único durante mucho tiempo. Por cierto, no se ha identificado el mecanismo del suicidio celular con una velocidad récord, en minutos. El segundo método se describió recientemente, los autores lo llamaron trogocitosis del griego "tres": roer. Es de destacar que las amebas que muerden las células abandonan a su presa tan pronto como muere. Otros pueden fagocitar las células muertas por completo. Se supone que las células que muerden y devoran difieren en el patrón de expresión génica.
Ahora, la capacidad de la ameba para penetrar en el torrente sanguíneo, el hígado y otros órganos está asociada con la trogocitosis.
La amebiasis es una enfermedad mortal, alrededor de 100 mil personas mueren por infección conE. histolyticacada año.
La ameba disentería tiene un gemelo no patógeno,E. dispar, por lo que la microscopía no es suficiente para diagnosticar la enfermedad.
Para curardebe destruirse como móvilE. histolyticay quistes.
DescribióE. histolyticay determinó su naturaleza patogénica en 1875 en un paciente con diarrea. El nombre latino de ameba fue dado en 1903 por el zoólogo alemán Fritz Schaudin.Histolyticasignifica destrucción de tejidos. En 1906, el científico murió a causa de un absceso intestinal amebiano.
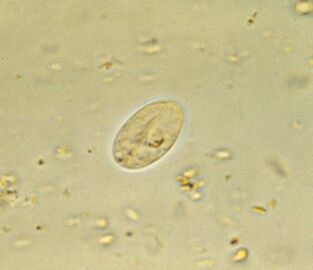
El más común. Lamblia intestinalGiardia lamblia (G. intestinalis)
Giardia, el parásito intestinal más común, es ubicuo. El 3-7% de las personas en los países desarrollados y el 20-30% en los países en desarrollo están infectados. Eso es alrededor de 300 millones de personas.
Los parásitos vivenen el duodeno y los conductos biliares del huésped, donde flotan, trabajando con flagelos, luego se adhieren al epitelio con la ayuda de un disco pegajoso ubicado en la parte inferior de la célula. Para 1 cm2, el epitelio se adhiere a un millón de lamblia. Dañan las vellosidades, lo que interfiere con la absorción de nutrientes, provocando inflamación de las mucosas y diarrea. Si la enfermedad afecta los conductos biliares, se acompaña de ictericia.
La giardiasis es una enfermedad de las manos, el agua y la comida sucias. El ciclo de vida de un protozoo es simple: en el intestino hay una forma activa y, a la salida, con masas fecales, quistes estables. Para infectarse, es suficiente tragar una docena de quistes, que en los intestinos volverán a convertirse en una forma activa.
El principal secretode la ubicuidad de lamblia en la variabilidad de las proteínas de superficie. El cuerpo humano lucha contra la lamblia con anticuerpos y, en principio, es capaz de desarrollar inmunidad. Pero las personas que viven en la misma zona y beben la misma agua se infectan una y otra vez por los descendientes de sus propios parásitos. ¿Por qué? Porque durante la transición de la fase activa al quiste y viceversa, lamblia cambia las proteínas para las que se producen los anticuerpos: proteínas de superficie específicas de variante. Hay alrededor de 190 variantes de estas proteínas en el genoma, pero solo una está siempre presente en la superficie de un parásito individual, la traducción del resto es interrumpida por el mecanismo de interferencia del ARN. Y el cambio ocurre aproximadamente una vez cada diez generaciones.
Se tratacon un agente antiprotozoario con actividad antibacteriana. La enfermedad desaparece en una semana, pero si los conductos biliares están infectados, es posible que se produzcan recaídas durante muchos años. Los quistes se combaten yodando el agua.
DescubiertaGiardia lambliaen 1859 por el científico checo Vilém Lambl. Desde entonces, el más simple ha cambiado varios nombres y el actual ha recibido en honor al descubridor y parasitólogo francés Alfred Giar, que no describió a lamblia.
Y el primer boceto de Giardia fue realizado por Anthony van Leeuwenhoek, quien lo encontró en su propia silla trastornada. Fue en 1681.
Por cierto, Giardia también es muy antigua desde el punto de vista evolutivo, proviene casi directamente del antepasado de todos los eucariotas.
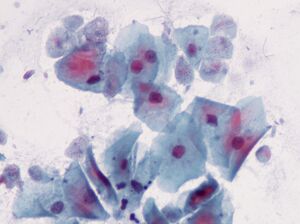
El más íntimo. Trichomonas vaginalisTrichomonas vaginalis.
El más simple, que se transmite sexualmente. Vive en la vagina y en los hombres; en la uretra, el epidídimo y la próstata, se transmite sexualmente o a través de paños húmedos. Los bebés pueden infectarse al pasar por el canal de parto.T. vaginalistiene 4 flagelos en el extremo anterior y una membrana ondulada relativamente corta; si es necesario, libera pseudópodos. El tamaño máximo de Trichomonas es de 32 por 12 micrones.
Trichomonas está másextendidoque los agentes causantes de clamidia, gonorrea y sífilis combinados. Afecta aproximadamente al 10% de las mujeres, y posiblemente a más, y al 1% de los hombres. Esta última cifra no es confiable porque es más difícil detectar el parásito en los hombres.
T. vaginalisse alimenta de microorganismos, incluidas las bacterias del ácido láctico de la microflora vaginal, que mantienen un ambiente ácido y, por lo tanto, crea un pH óptimo para sí mismo por encima de 4. 9.
Trichomonas destruye las células de la mucosa y causa inflamación. Aproximadamente el 15% de las mujeres infectadas se quejan de síntomas.
Se tratacon un fármaco antibacteriano. Como medida preventiva, se recomienda una ducha vaginal regular con vinagre diluido.
Descritoen 1836 por el bacteriólogo francés Alfred Donne. El científico no entendió que había un parásito patógeno frente a él, pero determinó el tamaño, apariencia y tipo de movimiento de los más simples.
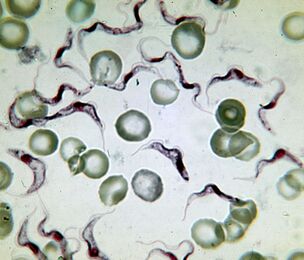
El más mortífero. El agente causante de la enfermedad del sueñoTrypanosoma brucei
El agente causante de la enfermedad del sueño africana es el protozoo más mortífero. Una persona infectada muere sin tratamiento. El tripanosoma es un flagelado alargado de 15 a 40 µm de longitud. Se conocen dos subespecies que son aparentemente indistinguibles. Enfermedad causada porT. brucei gambiense, dura de 2 a 4 años.T. brucei rhodesiensees un patógeno transitorio más virulento del cual mueren después de unos meses o semanas.
Distribuidoen África, entre los 15 paralelos de los hemisferios sur y norte, en el rango natural del portador: insectos chupadores de sangre del géneroGlossina(mosca tsetsé). De las 31 especies de moscas, 11 son peligrosas para los seres humanos La enfermedad del sueño afecta a la población de 37 países al sur del Sahara a 9 millones de km2. Hasta 20 mil personas enferman cada año. Ahora hay unos 500 mil pacientes, 60 millones viven en riesgo.
Desde el intestino de la moscaT. bruceiingresa al torrente sanguíneo humano, desde allí ingresa al líquido cefalorraquídeo y afecta el sistema nervioso. La enfermedad comienza con fiebre e inflamación de los ganglios linfáticos, seguida de letargo, somnolencia, parálisis muscular, agotamiento y coma irreversible.
La letalidad del parásito está asociada con su capacidad para cruzar la barrera hematoencefálica. Los mecanismos moleculares no se comprenden completamente, pero se sabe que cuando ingresa al cerebro, el parásito secreta cisteína proteasas y también usa algunas proteínas del huésped. En el sistema nervioso central, en cambio, el tripanosoma se refugia de factores inmunes.
La primera descripción de la enfermedad del sueño en la parte alta del Níger la dejó el erudito árabe Ibn Jaldún (1332-1406). A principios del siglo XIX, los europeos ya conocían bien el signo inicial de la enfermedad: hinchazón de los ganglios linfáticos en la parte posterior del cuello (un síntoma de Winterbottom), y los traficantes de esclavos le prestaron especial atención.
DescubrióT. bruceiEl microbiólogo escocés David Bruce, de quien lleva su nombre, y en 1903 estableció por primera vez la conexión entre el tripanosoma, la mosca tsetsé y la enfermedad del sueño.
El tratamientodepende del estadio de la enfermedad y los medicamentos causan efectos secundarios graves. El parásito tiene una alta variabilidad antigénica, por lo que es imposible crear una vacuna.
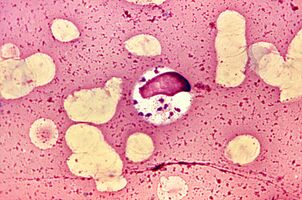
El más extravagante. LeishmaniaLeishmania donovani
Las leishmanias se han ganado el título de los parásitos más extravagantes porque viven y se reproducen en macrófagos, células diseñadas para destruir parásitos.L. donovanies el más peligroso de ellos. Causa leishmaniasis visceral, coloquialmente fiebre dumdum o kala azar, de la que casi todos los pacientes mueren sin tratamiento. Pero los supervivientes adquieren inmunidad a largo plazo.
Hay tres subespecies del parásito.L. donovani infantum(Mediterráneo y Asia central) afecta principalmente a los niños, los perros suelen ser su reservorio.L. donovani donovani(India y Bangladesh) es peligrosa para adultos y ancianos, no tiene reservorios naturales. ElL. donovani chagasiamericano (América Central y del Sur) puede vivir en la sangre de los perros.
L. donovani- flagelado de no más de 6 micrones de longitud. Las personas se infectan después de ser picadas por mosquitos del géneroPhlebotomus, a veces a través del contacto sexual, bebés, que pasan por el canal de parto. Una vez en la sangre,L. donovanipenetra en los macrófagos, que transportan el parásito a través de los órganos internos. Al reproducirse en macrófagos, el parásito los destruye. El mecanismo molecular de supervivencia en los macrófagos es bastante complejo.
Síntomas de la enfermedad: fiebre, agrandamiento del hígado y el bazo, anemia y leucopenia, que contribuyen a la infección bacteriana secundaria. Cada año 500 mil personas enferman de leishmaniasis visceral y mueren unas 40 mil.
Tratamientopesado: antimonio intravenoso y transfusión de sangre.
La afiliación taxonómicaL. donovanifue determinada en 1903 por el famoso investigador de la malaria y premio Nobel Ronald Ross. Debe su nombre genérico a William Leishman, y el nombre específico a Charles Donovan, quien en el mismo 1903 descubrió independientemente células protozoarias en el bazo de pacientes que murieron por kala azar, uno en Londres, el otro en Madrás.
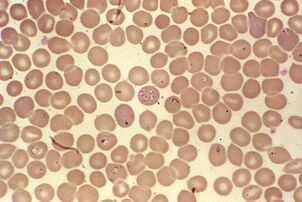
El ciclo de vida más difícil.Babesia spp.
Las babesias, además de la reproducción asexual de múltiples etapas en eritrocitos de mamíferos y ácaros sexuales en los intestinos del géneroIxodes, complicaron su desarrollo por transmisión transovárica. Desde los intestinos de un ácaro hembra, los esporozoitos protozoarios penetran en los ovarios e infectan a los embriones. Cuando las larvas del ácaro eclosionan, la babesia pasa a sus glándulas salivales y, con el primer mordisco, entra en la sangre del vertebrado.
DistribuidoBabesia en América, Europa y Asia. Su reservorio natural son los roedores, perros y ganado. Una persona está infectada con varios tipos: B. microti, B. divergens, B. duncaniyB. venatorum.
Los síntomas de la babesiosis son similares a los de la malaria: fiebre recurrente, anemia hemolítica, agrandamiento del bazo e hígado. La mayoría de las personas se recuperan espontáneamente, pero la babesiosis es fatal para los pacientes con sistemas inmunitarios debilitados.
Los métodos de tratamientoaún están en desarrollo, mientras que se prescriben antibióticos y, en casos graves, transfusiones de sangre.
Babesia fue descrita por el microbiólogo rumano Victor Babes (1888), quien la descubrió en vacas y ovejas enfermas. Decidió que estaba tratando con una bacteria patógena que llamóHaematococcus bovis. La babesia se consideró durante mucho tiempo un patógeno animal hasta que se descubrió en 1957 en un pastor yugoslavo que murió de una infección por B. divergens.
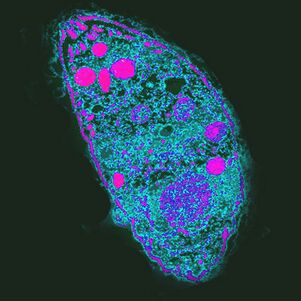
El más influyente. El agente causante de la toxoplasmosisToxoplasma gondii
T. gondiies el parásito más poderoso ya que controla el comportamiento de los huéspedes intermediarios.
Distribuidoen todas partes, distribuido de manera desigual. En Francia, por ejemplo, el 84% de la población está infectada, en el Reino Unido, el 22%.
El ciclo de vida del Toxoplasma consta de dos etapas: el asexual ocurre en el cuerpo de cualquier sangre caliente, la reproducción sexual es posible solo en las células epiteliales del intestino del gato. AT. gondiipodría completar el desarrollo, el gato debe comer un roedor infectado. Al aumentar la probabilidad de este evento,T. gondiibloquea el miedo natural de los roedores al olor a orina de gato y lo hace atractivo al dirigirse a un grupo de neuronas en la amígdala. Se desconoce cómo lo hace. Uno de los supuestos mecanismos de acción es una respuesta inmune local a la infección. Altera los niveles de citocinas, lo que a su vez eleva los niveles de neuromoduladores como la dopamina. El toxoplasma también afecta el comportamiento humano, que se manifiesta incluso a nivel poblacional. Entonces, en países con un alto nivel de toxoplasmosis, neuroticismo y el deseo de evitar la incertidumbre, las situaciones nuevas son más comunes. Es posible que la infección porT. gondiipueda provocar cambios culturales.
La infecciónen los seres humanos suele ser asintomática, pero con la inmunidad debilitada destruye las células del hígado, los pulmones, el cerebro y la retina, provocando toxoplasmosis aguda o crónica. El curso de la infección depende de la virulencia de la cepa, el estado del sistema inmunológico del huésped y su edad; las personas mayores son menos susceptibles aT. gondii.
Tratela toxoplasmosis con medicamentos antiprotozoarios.
Descritoen 1908 en roedores del desierto. Este honor pertenece al personal del Instituto Pasteur de Túnez, Charles Nicolas y Luis Manso.
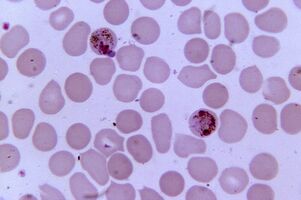
Más patógeno. Paludismo por PlasmodiumPlasmodium spp.
La malaria por Plasmodium es el parásito más patógeno en los seres humanos. El número de pacientes con malaria puede llegar a 300-500 millones, y la tasa de mortalidad durante las epidemias - 2 millones. La enfermedad todavía se cobra tres veces más vidas que los conflictos armados.
Cinco tipos de Plasmodium causan paludismo en humanos:Plasmodium vivax, P. falciparum, P. malariae, P. ovaleyP. knowlesi, que también afecta a los macacos.
Distribuidosen la gama de vectores: mosquitosAnopheles, que necesitan una temperatura de 16–34 ° C y una humedad relativa de más del 60%.
La comparación del genoma del plasmodio más virulento,P. falciparum, con el plasmodio del gorila sugiere que los humanos fueron infectados por su ancestro de estos monos. El surgimiento de esta forma de Plasmodium está asociado con el surgimiento de la agricultura en África, lo que condujo a un aumento de la densidad de población y al desarrollo de sistemas de riego.
La reproducción sexual de plasmodios ocurre en los intestinos de los mosquitos, y en el cuerpo humano es un parásito intracelular que vive y se reproduce en los hepatocitos y eritrocitos hasta que las células estallan. 1 ml de sangre del paciente contiene 1 - 50 mil parásitos.
La enfermedad se manifiesta como inflamación, fiebre recurrente y anemia, en caso de embarazo es peligrosa para la madre y el feto. Los eritrocitos infectados conP. falciparumobstruyen los capilares y, en casos graves, se desarrolla isquemia de órganos y tejidos internos.
El tratamientorequiere una combinación de varios medicamentos y depende del patógeno específico. Los plasmodios se vuelven resistentes a las drogas.








































